a greener, simpler way to create syngas
UCLA and Rice researchers develope new method to produce vital industrial gas
onderzoekers van UCLA Samueli School of Engineering, Rice University en UC Santa Barbara hebben een eenvoudiger en groenere manier ontwikkeld om syngas te maken.
een studie over hun werk wordt vandaag gepubliceerd in Nature Energy.
Syngas (“synthesegas”) is een mengsel van koolmonoxide en waterstofgas. Het wordt gebruikt om ammoniak, methanol, andere industriële chemicaliën en brandstoffen te maken. Het meest voorkomende proces voor het maken van syngas is kolenvergassing, waarbij stoom en zuurstof (uit lucht) bij hoge temperaturen worden gebruikt, een proces dat grote hoeveelheden kooldioxide produceert.
een andere milieuvriendelijke manier om syngas te maken, methaan droog reformeren genaamd, bestaat erin om twee krachtige broeikasgassen te laten reageren-methaan (bijvoorbeeld uit aardgas) en kooldioxide. Maar dat proces wordt niet veel gebruikt op industriële schaal, mede omdat het temperaturen van ten minste 1300 graden Fahrenheit (700 graden Celsius) vereist om de chemische reactie in gang te zetten.
de afgelopen tien jaar hebben onderzoekers geprobeerd het proces voor het maken van syngas te verbeteren met behulp van verschillende metaallegeringen die de vereiste chemische reactie bij lagere temperaturen zouden kunnen katalyseren. Maar de tests waren ofwel inefficiënt of resulteerden in de metaalkatalysatoren bedekt met cokes, een residu van voornamelijk koolstof dat zich opbouwt tijdens het proces.
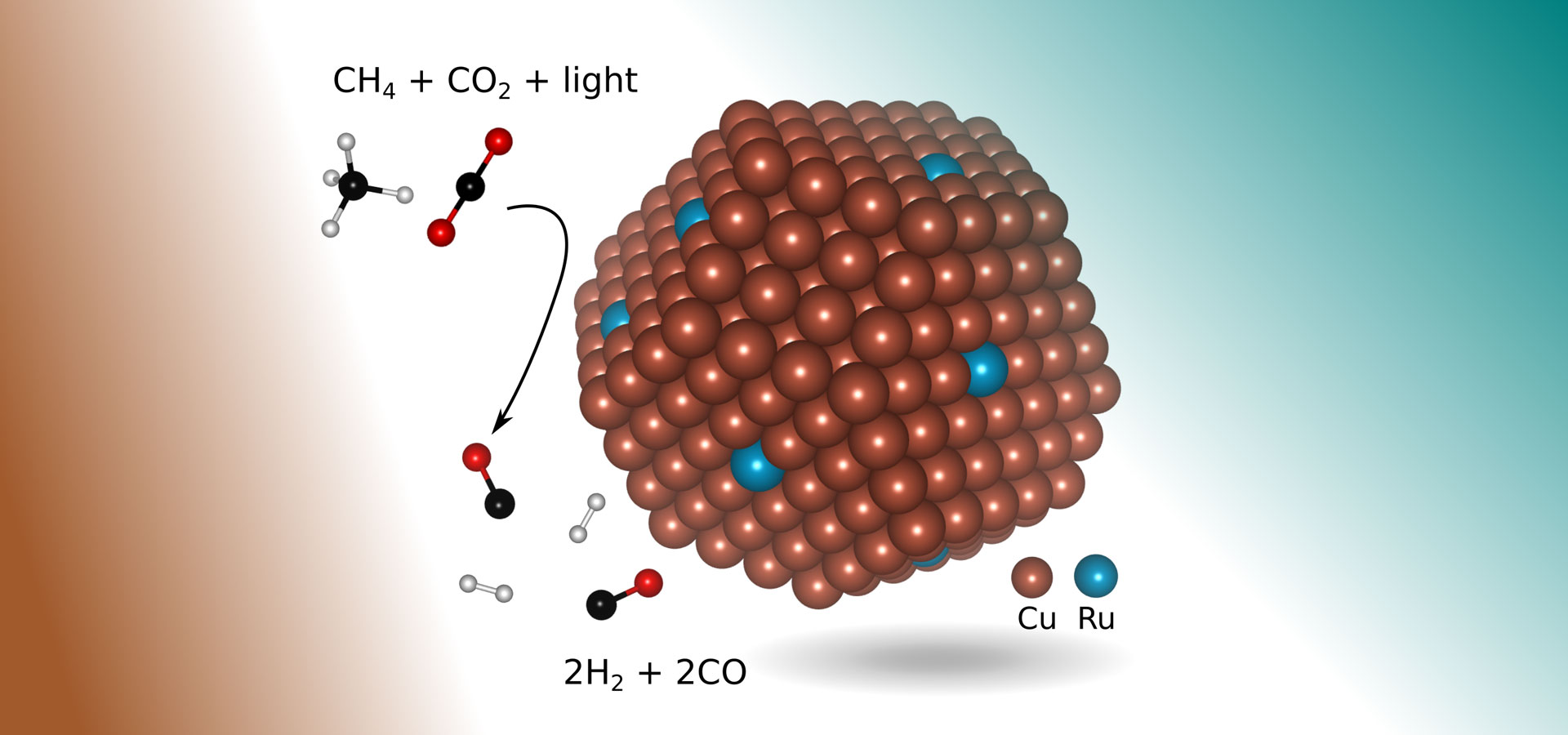
in het nieuwe onderzoek vonden ingenieurs een meer geschikte katalysator: koper met enkele atomen van het edelmetaalruthenium blootgesteld aan zichtbaar licht. In de vorm van een kleine bult van ongeveer 5 nanometer in diameter (een nanometer is een miljardste van een meter) en liggend op een metaaloxide ondersteuning, maakt de nieuwe katalysator een chemische reactie mogelijk die selectief syngas produceert uit de twee broeikasgassen met behulp van zichtbaar licht om de reactie aan te sturen, zonder dat er extra thermische energie-input nodig is.
bovendien vereist het proces in principe alleen geconcentreerd zonlicht, waardoor ook de vorming van cokes die eerdere methoden teisterde, wordt voorkomen.
 ” Syngas wordt alom gebruikt in de chemische industrie om veel chemicaliën en materialen te creëren die ons dagelijks leven mogelijk maken,” zei Emily Carter, een UCLA distinguished professor of chemical and biomolecular engineering, en een corresponderende auteur van het artikel. “Wat spannend is aan dit nieuwe proces is dat het de mogelijkheid biedt om opgevangen broeikasgassen te reageren — het verminderen van koolstofemissies naar de atmosfeer — terwijl het creëren van deze kritische chemische grondstof met behulp van een goedkope katalysator en hernieuwbare energie in de vorm van zonlicht in plaats van het gebruik van fossiele brandstoffen.”
” Syngas wordt alom gebruikt in de chemische industrie om veel chemicaliën en materialen te creëren die ons dagelijks leven mogelijk maken,” zei Emily Carter, een UCLA distinguished professor of chemical and biomolecular engineering, en een corresponderende auteur van het artikel. “Wat spannend is aan dit nieuwe proces is dat het de mogelijkheid biedt om opgevangen broeikasgassen te reageren — het verminderen van koolstofemissies naar de atmosfeer — terwijl het creëren van deze kritische chemische grondstof met behulp van een goedkope katalysator en hernieuwbare energie in de vorm van zonlicht in plaats van het gebruik van fossiele brandstoffen.”
Carter is ook UCLA ‘ s uitvoerend vicekanselier en Provoost.
John Mark Martirez, een UCLA assistant Project scientist, voerde de kwantummechanische analyse van de reactie uit, waarbij het stap-voor-stap, atoom-voor-atoom proces werd aangetoond van de chemische reactie die de gassen creëert.De eerste auteur van de studie is Linan Zhou, een postdoctoraal onderzoeker aan de Universiteit van Rice. Andere senior auteurs zijn professoren van Rice, Naomi Halas en Peter Nordlander, en van UC Santa Barbara, onder leiding van Phillip Christopher.Het onderzoek werd ondersteund door de Air Force Office of Scientific Research via het Department of Defense multidisciplinary university research initiative program en door de Welch Foundation, die fundamenteel onderzoek in de chemie ondersteunt.