zelenější, jednodušší způsob, jak vytvořit syngas
UCLA a Rice vědci vyvinout novou metodu k výrobě životně důležité průmyslový plyn
výzkumníci z UCLA Samueli School of Engineering, Rice University a UC Santa Barbara vyvinuli jednodušší a zelenější způsob, jak vytvořit syngas.
studie popisující jejich práci je dnes zveřejněna v Nature Energy.
Syngas (termín je zkratka pro „syntézní plyn“) je směs oxidu uhelnatého a plynů vodíku. Používá se k výrobě amoniaku, methanolu, jiných průmyslových chemikálií a paliv. Nejběžnějším procesem vytváření syngasu je zplyňování uhlí, které využívá páru a kyslík (ze vzduchu) při vysokých teplotách, což je proces, který produkuje velké množství oxidu uhličitého.
jedním z ekologičtějších způsobů, jak vytvořit syngas, zvaný suché reformování metanu, je získání dvou silných skleníkových plynů, které reagují — metanu (například ze zemního plynu) a oxidu uhličitého. Tento proces však není široce používán v průmyslových měřítcích, částečně proto, že k zahájení chemické reakce vyžaduje teploty nejméně 1300 stupňů Fahrenheita (700 stupňů Celsia).
během posledního desetiletí se vědci pokusili zlepšit proces vytváření syngasů pomocí různých kovových slitin, které by mohly katalyzovat požadovanou chemickou reakci při nižších teplotách. Testy však byly buď neúčinné, nebo vedly k tomu, že kovové katalyzátory byly pokryty koksem, zbytek převážně uhlíku, který se během procesu hromadí.
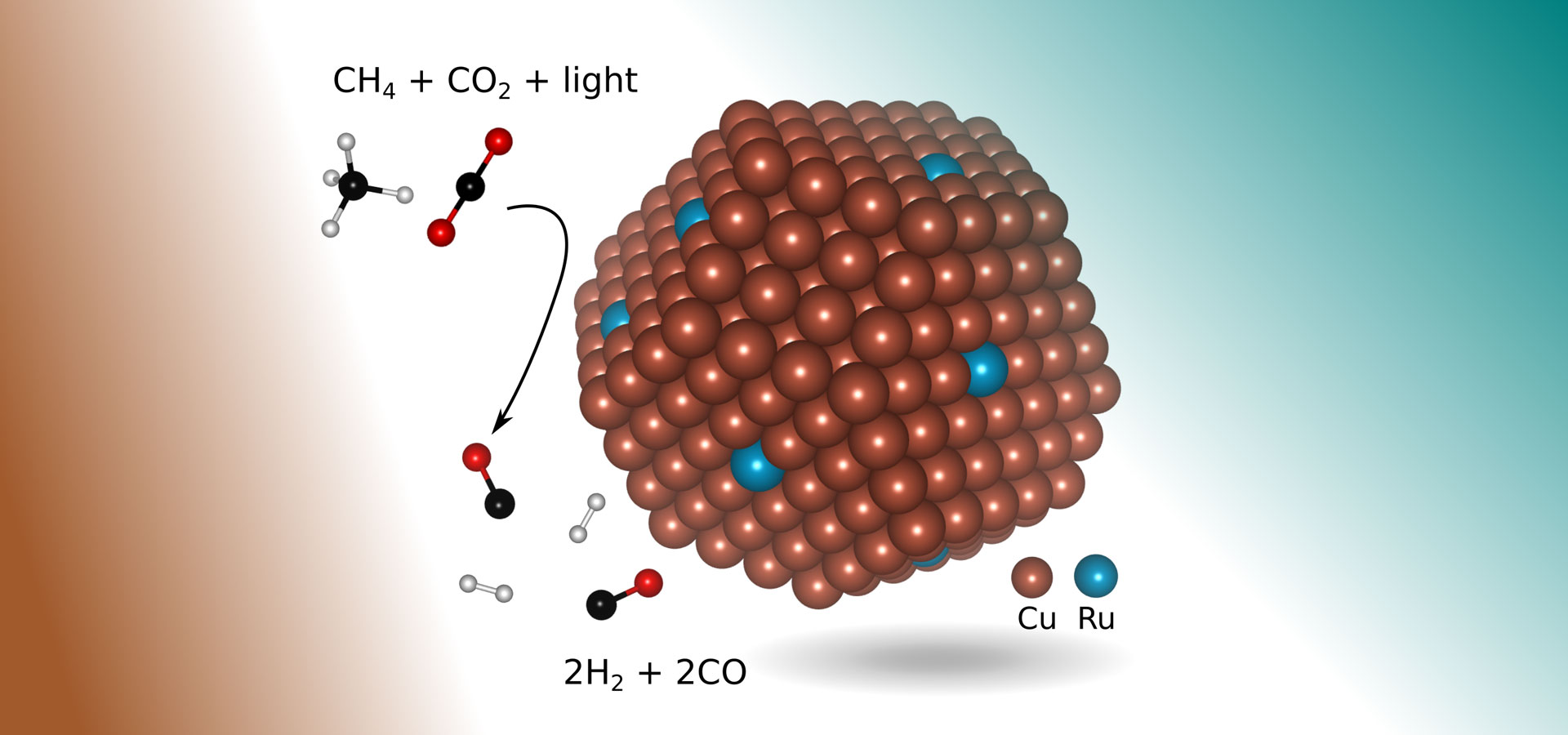
v novém výzkumu našli inženýři vhodnější katalyzátor: měď s několika atomy ruthenia drahého kovu vystavenými viditelnému světlu. Nový katalyzátor, tvarovaný jako malý náraz o průměru asi 5 nanometrů (nanometr je jedna miliardtina metru) a ležící na horní části nosiče oxidu kovu, umožňuje chemickou reakci, která selektivně produkuje syngas ze dvou skleníkových plynů pomocí viditelného světla k řízení reakce, aniž by vyžadoval další vstup tepelné energie.
kromě toho proces v zásadě vyžaduje pouze koncentrované sluneční světlo, které také zabraňuje hromadění koksu, který trápil dřívější metody.
 „Syngas se v chemickém průmyslu používá všudypřítomně k vytvoření mnoha chemikálií a materiálů, které umožňují náš každodenní život,“ řekla Emily Carterová, profesorka chemického a biomolekulárního inženýrství UCLA a odpovídající autor článku. „Na tomto novém procesu je vzrušující to, že nabízí příležitost reagovat zachycené skleníkové plyny-snižovat emise uhlíku do atmosféry-a zároveň vytvářet tuto kritickou chemickou surovinu pomocí levného katalyzátoru a obnovitelné energie ve formě slunečního světla místo používání fosilních paliv.“
„Syngas se v chemickém průmyslu používá všudypřítomně k vytvoření mnoha chemikálií a materiálů, které umožňují náš každodenní život,“ řekla Emily Carterová, profesorka chemického a biomolekulárního inženýrství UCLA a odpovídající autor článku. „Na tomto novém procesu je vzrušující to, že nabízí příležitost reagovat zachycené skleníkové plyny-snižovat emise uhlíku do atmosféry-a zároveň vytvářet tuto kritickou chemickou surovinu pomocí levného katalyzátoru a obnovitelné energie ve formě slunečního světla místo používání fosilních paliv.“
Carter je také výkonným vicekancléřem a proboštem UCLA.
John Mark Martirez, pomocný projektový vědec UCLA, provedl kvantovou mechanickou analýzu reakce a ukázal krok za krokem proces chemické reakce, která vytváří plyny.
prvním autorem studie je Linan Zhou, postdoktorand v Rice. Dalšími významnými autory jsou profesoři z Rice, Naomi Halas a Peter Nordlander a z UC Santa Barbara, vedeni Phillipem Christopherem.
výzkum byl podpořen letectvem Úřadu vědeckého výzkumu prostřednictvím ministerstva obrany multidisciplinární university research initiative program, a Welch Foundation, která podporuje základní výzkum v chemii.