A greener, simpler way to create syngas
UCLA und Reis Forscher entwickeln neue Methode zur Herstellung von lebenswichtigem Industriegas
Forscher der UCLA Samueli School of Engineering, der Rice University und der UC Santa Barbara haben eine einfachere und umweltfreundlichere Methode zur Herstellung von Synthesegas entwickelt.
Eine Studie, die ihre Arbeit detailliert beschreibt, wird heute in Nature Energy veröffentlicht.
Synthesegas (der Begriff ist kurz für „Synthesegas“) ist eine Mischung aus Kohlenmonoxid und Wasserstoffgasen. Es wird zur Herstellung von Ammoniak, Methanol, anderen Industriechemikalien und Kraftstoffen verwendet. Das gebräuchlichste Verfahren zur Erzeugung von Synthesegas ist die Kohlevergasung, bei der Dampf und Sauerstoff (aus Luft) bei hohen Temperaturen verwendet werden.
Eine weitere umweltfreundliche Methode zur Erzeugung von Synthesegas, die als Methan—Trockenreformierung bezeichnet wird, besteht darin, zwei starke Treibhausgase zur Reaktion zu bringen – Methan (z. B. aus Erdgas) und Kohlendioxid. Dieser Prozess wird jedoch im industriellen Maßstab nicht häufig verwendet, zum Teil, weil er Temperaturen von mindestens 1.300 Grad Fahrenheit (700 Grad Celsius) erfordert, um die chemische Reaktion auszulösen.
In den letzten zehn Jahren haben Forscher versucht, den Prozess zur Herstellung von Synthesegas unter Verwendung verschiedener Metalllegierungen zu verbessern, die die erforderliche chemische Reaktion bei niedrigeren Temperaturen katalysieren könnten. Die Tests waren jedoch entweder ineffizient oder führten dazu, dass die Metallkatalysatoren mit Koks bedeckt waren, einem Rückstand aus hauptsächlich Kohlenstoff, der sich während des Prozesses ansammelt.
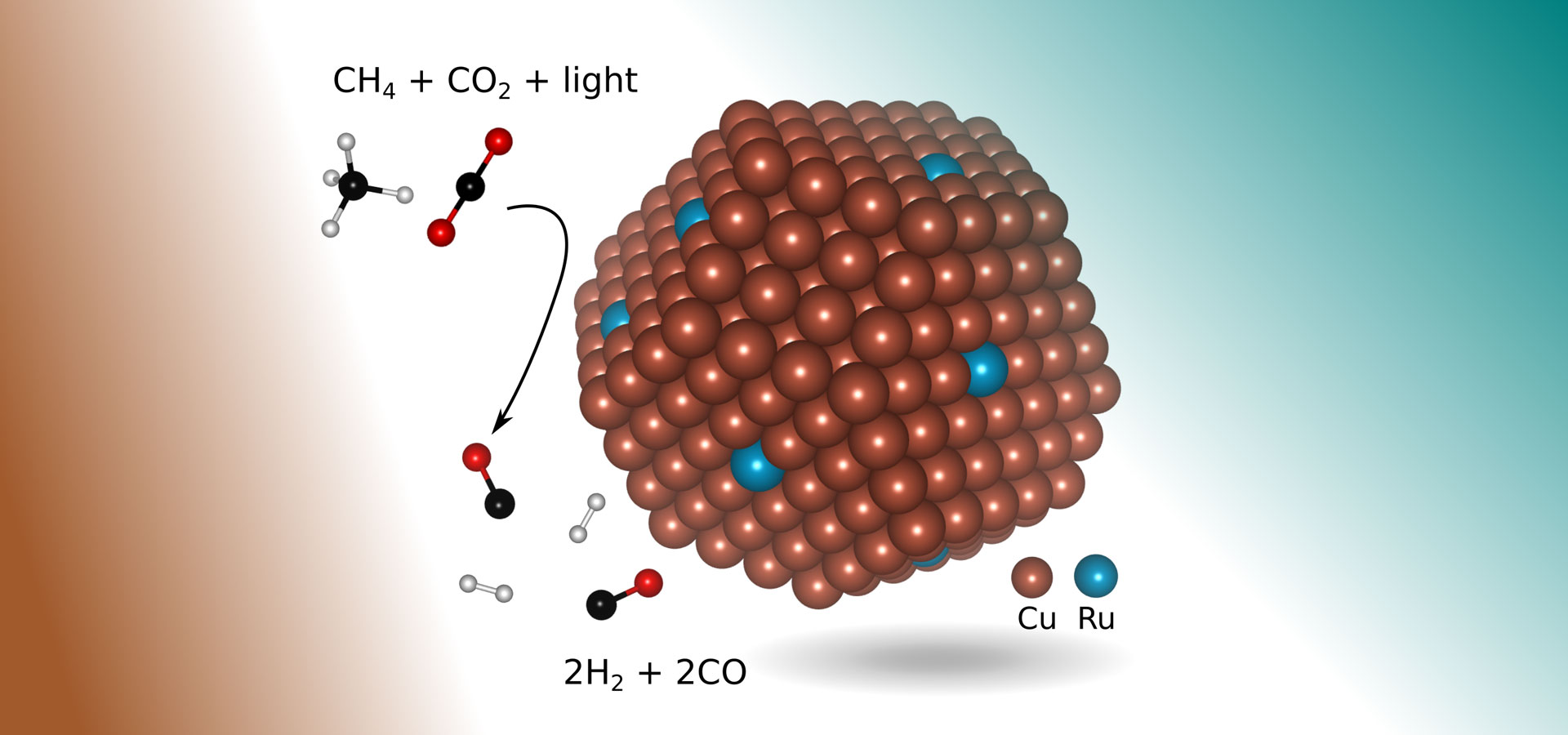
In der neuen Forschung fanden die Ingenieure einen geeigneteren Katalysator: Kupfer mit einigen Atomen des Edelmetalls Ruthenium, die sichtbarem Licht ausgesetzt waren. Der neue Katalysator, der wie eine winzige Beule mit einem Durchmesser von etwa 5 Nanometern geformt ist (ein Nanometer ist ein Milliardstel Meter) und auf einem Metalloxidträger liegt, ermöglicht eine chemische Reaktion, bei der selektiv Synthesegas aus den beiden Treibhausgasen erzeugt wird sichtbares Licht, um die Reaktion anzutreiben, ohne zusätzlichen Wärmeenergieeinsatz zu erfordern.
Darüber hinaus benötigt das Verfahren im Prinzip nur konzentriertes Sonnenlicht, wodurch auch die Bildung von Koks verhindert wird, die frühere Methoden plagte.
 „Synthesegas wird in der chemischen Industrie allgegenwärtig verwendet, um viele Chemikalien und Materialien herzustellen, die unser tägliches Leben ermöglichen“, sagte Emily Carter, eine angesehene Professorin für Chemie und Biomolekulartechnik an der UCLA und korrespondierende Autorin des Papiers. „Das Spannende an diesem neuen Verfahren ist, dass es die Möglichkeit bietet, auf Treibhausgase zu reagieren — die Kohlenstoffemissionen in die Atmosphäre zu reduzieren — und gleichzeitig diesen kritischen chemischen Rohstoff mit einem kostengünstigen Katalysator und erneuerbarer Energie in Form von Sonnenlicht anstelle fossiler Brennstoffe zu erzeugen.“
„Synthesegas wird in der chemischen Industrie allgegenwärtig verwendet, um viele Chemikalien und Materialien herzustellen, die unser tägliches Leben ermöglichen“, sagte Emily Carter, eine angesehene Professorin für Chemie und Biomolekulartechnik an der UCLA und korrespondierende Autorin des Papiers. „Das Spannende an diesem neuen Verfahren ist, dass es die Möglichkeit bietet, auf Treibhausgase zu reagieren — die Kohlenstoffemissionen in die Atmosphäre zu reduzieren — und gleichzeitig diesen kritischen chemischen Rohstoff mit einem kostengünstigen Katalysator und erneuerbarer Energie in Form von Sonnenlicht anstelle fossiler Brennstoffe zu erzeugen.“
Carter ist auch Executive Vice Chancellor und Provost der UCLA.
John Mark Martirez, ein UCLA Assistant Project Scientist, führte die quantenmechanische Analyse der Reaktion durch und zeigte den schrittweisen Atom-für-Atom-Prozess der chemischen Reaktion, die die Gase erzeugt.
Der Erstautor der Studie ist Linan Zhou, ein Postdoktorand bei Rice. Weitere leitende Autoren sind Professoren von Rice, Naomi Halas und Peter Nordlander sowie von der UC Santa Barbara unter der Leitung von Phillip Christopher.
Die Forschung wurde vom Air Force Office of Scientific Research über das Programm der multidisziplinären Universitätsforschungsinitiative des Verteidigungsministeriums und von der Welch Foundation unterstützt, die Grundlagenforschung in der Chemie unterstützt.