sztuczne serce
Informacje ogólne
naturalne serce ma dwie pompy, każda z dwiema komorami. Prawy przedsionek pompuje krew pozbawioną tlenu z organizmu do prawej komory, która pompuje ją do płuc. Lewy przedsionek wysyła napowietrzoną krew z płuc do lewej komory, która pompuje ją do ciała. Z każdym biciem serca, dwa przedsionki kurczą się razem, a następnie dużych komór.
zastoinowa niewydolność serca, która jest stale zmniejszającą się zdolnością serca do pompowania krwi, jest jedną z głównych przyczyn śmierci. Choroba ta jest spowodowana nagłym uszkodzeniem w wyniku zawałów serca, pogorszeniem się infekcji wirusowych, nieprawidłowym działaniem zastawek, wysokim ciśnieniem krwi i innymi problemami. Według American Heart Association szacuje się, że pięć milionów Amerykanów żyje z niewydolnością serca, a ponad 400 000 nowych przypadków jest diagnozowanych każdego roku. Około 50% wszystkich pacjentów umiera w ciągu pięciu lat. Choroby serca kosztowały amerykański przemysł zdrowotny około 95 miliardów dolarów w 1998 roku.
chociaż leki i techniki chirurgiczne mogą pomóc w kontrolowaniu objawów, jedynym lekarstwem na niewydolność serca jest przeszczep narządów. W 1998 roku około 7700 Amerykanów było na krajowej liście przeszczepów serca, ale tylko 30% otrzymało przeszczepy. Sztuczne serca i urządzenia wspomagające pompowanie zostały opracowane jako potencjalne alternatywy.
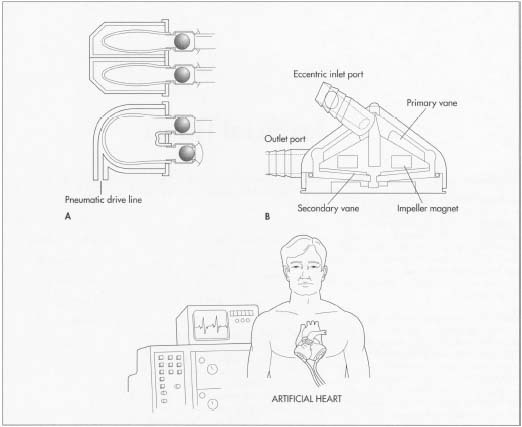
sztuczne serce utrzymuje krążenie krwi i dotlenienie serca przez różne okresy czasu. Idealne sztuczne serce musi bić 100 000 razy co 24 godziny bez konieczności smarowania ani konserwacji i musi mieć stałe źródło zasilania. Musi również pompować szybciej lub wolniej, w zależności od aktywności pacjenta, bez powodowania infekcji lub skrzepów krwi.
dwa główne typy sztucznych serc to maszyna sercowo-płucna i serce mechaniczne. Pierwszy typ składa się z dotleniacza i pompy i służy głównie do utrzymywania przepływu krwi podczas operacji serca. Ta maszyna może działać tylko przez kilka godzin, ponieważ krew ulega uszkodzeniu po dłuższym czasie.
serce mechaniczne jest zaprojektowane w celu zmniejszenia całkowitego obciążenia pracą serca, które nie może już pracować w normalnej pojemności. Serca te składają się z urządzeń, które pulsuje krew między uderzeniami serca lub użyć sztucznej Komory pomocniczej (urządzenie wspomagające lewą komorę, LVAD), która pompuje część normalnej pojemności minutowej serca. Ponieważ takie urządzenia zwykle powodują powikłania dla pacjenta, na ogół były one używane jako tymczasowe zastępstwo, dopóki naturalne serca mogą być uzyskane do przeszczepu. Na całym świecie wszczepiono około 4000 LVAD. Rynek tych urządzeń szacuje się na 12 miliardów dolarów rocznie w Stanach Zjednoczonych.
Historia
od końca XIX wieku naukowcy próbowali opracować urządzenie mechaniczne, które mogłoby przywrócić tlen do krwi i usunąć nadmierny dwutlenek węgla, a także pompę, która tymczasowo zastąpiłaby działanie serca. Minęło prawie 100 lat, zanim w 1953 roku John H. Gibbon Jr.użył na człowieku pierwszej udanej maszyny serca i płuc. Cztery lata później pierwsze sztuczne serce (wykonane z tworzywa sztucznego) w świecie zachodnim zostało wszczepione do wnętrza psa. Narodowy Instytut Serca
założył program sztucznego serca w 1964 roku, prowadząc do pierwszego całkowitego sztucznego serca do użytku ludzkiego wszczepionego w 1969 roku.
w 1970 r.nacisk został przesunięty na systemy wspomagania lewej komory i materiały kompatybilne z krwią. W tym samym roku z powodzeniem zastosowano LVAD. Jednak rozwój pompy krwi kontynuował i urządzenia stały się mniejsze, lżejsze, bardziej akceptowalne i klinicznie skuteczne. Opracowano również szereg pomp poliuretanowych i plastikowych o długiej żywotności. W latach 80. Food and Drug Administration (FDA) nałożyła bardziej restrykcyjne przepisy na ustawę o standardach wyrobów medycznych, co doprowadziło do wyższych kosztów rozwoju. Wiele grup badawczych musiało się wycofać, a do dziś pozostało tylko kilka.
chyba najbardziej znanym naukowcem jest dr Robert Jarvik, który wynalazł sztuczne serce zwane Jarvik-7. To urządzenie, wykonane z aluminium i Tworzywa Sztucznego, zastąpiło dwie dolne komory naturalnego serca i wykorzystało dwie gumowe membrany do pompowania. Zewnętrzny kompresor wielkości lodówki utrzymywał sztuczne bicie serca. Barney Clark był pierwszym pacjentem, który otrzymał to serce. Przeżył 112 dni zanim fizyczne komplikacje wywołane implantem odebrały mu życie. W 1986 roku William Schroeder został drugim odbiorcą Jarvik-7, który przetrwał około 20 miesięcy.
społeczność medyczna zdała sobie sprawę, że całkowicie wszczepialne serce może uniknąć problemów z poruszaniem się i infekcją spowodowanych przez Jarvik-7. W 1988 roku National Institutes of Health rozpoczął finansowanie rozwoju takich serc i był wspieranie takiego programu w 1991 roku o łącznej wartości 6 milionów dolarów. Trzy lata później dostępny był wszczepialny LVAD zasilany elektrycznie i bateryjnie. W 1999 roku Charlie Chappis został pierwszym pacjentem wypuszczonym ze szpitala z takim urządzeniem. Inne sztuczne serca o różnych wzorach są obecnie testowane.
surowce
sztuczne serce lub LVAD jest wykonane z części metalowych, plastikowych, ceramicznych i zwierzęcych. Stop tytan-aluminium-wanad jest stosowany do pompy i innych części metalowych, ponieważ jest biokompatybilny i ma odpowiednie właściwości strukturalne. Części tytanowe są odlewane w specjalistycznym procesorze tytanowym. Z wyjątkiem powierzchni kontaktujących się z krwią, tytan jest obrabiany do określonego wykończenia. Powierzchnie mające kontakt z krwią otrzymują specjalną powłokę z mikrosfer tytanowych, które trwale łączą się z powierzchnią. Dzięki tej powłoce komórki krwi przylegają do powierzchni, tworząc żywą podszewkę.
membrana kontaktująca się z krwią w pompie jest wykonana ze specjalnego rodzaju poliuretanu, który jest również teksturowany, aby zapewnić przyleganie komórek krwi. Dwa rurowe przeszczepy są wykonane z poliestru (które są używane do przymocowania urządzenia do aorty), a zawory są rzeczywistymi zastawkami serca usuniętymi ze świni. Inne części, które tworzą silnik, są wykonane z tytanu lub innych metali i ceramiki.
projekt
istnieje kilka krytycznych problemów podczas projektowania LVAD. Dynamika płynów w przepływie krwi musi być rozumiana tak, aby wystarczająca ilość krwi była pompowana i nie powstawały skrzepy krwi. Należy wybrać materiały, które są biokompatybilne; w przeciwnym razie pompa może ulec awarii. Wydajność silnika musi być zoptymalizowana tak, aby generowane było minimalne ciepło. Z powodu możliwego odrzucenia całkowita objętość i pole powierzchni całego urządzenia powinny być jak najmniejsze. Typowy LVAD waży około 2,4 funta (1200 gm) i ma objętość 1,4 litra (660 ml).
Robert Jarvik urodził się 11 maja 1946 roku w Midland w stanie Michigan, a dorastał w Stamford w stanie Connecticut. W 1964 wstąpił na nowojorski Syracuse University, studiując architekturę i rysunek mechaniczny. Po tym, jak jego ojciec zachorował na chorobę serca, Jarvik przeszedł na leczenie wstępne. Ukończył studia w 1968 roku z tytułem bachelor of arts w dziedzinie zoologii, ale został odrzucony przez szkoły medyczne w Stanach Zjednoczonych. Wstąpił na Uniwersytet Boloński we Włoszech, ale w 1971 wyjechał na New York University, zdobywając tytuł master of arts w dziedzinie biomechaniki zawodowej.
Jarvik złożył podanie o pracę na Uniwersytecie Utah. Dyrektor Instytutu Inżynierii Biomedycznej I Wydziału sztucznych narządów, Willem Kolff, rozwijał sztuczne serce od połowy lat 50. Jarvik rozpoczął pracę jako asystent laboratoryjny, zdobywając dyplom medyczny w 1976 roku.
2 grudnia 1982 roku lekarze przeszczepili człowiekowi pierwsze sztuczne serce. To plastikowe i aluminiowe urządzenie, Jarvik-7, zostało wszczepione Barneyowi Clarkowi, który przeżył 112 dni po operacji. Kilku innych pacjentów otrzymywało Jarvik-7 serc, ale żaden nie żył dłużej niż 620 dni. Głównymi korzyściami było to, że nie będzie czekać na ludzkie serce i nie będzie szans na odrzucenie. Oczywistą pułapką jest to, że pacjenci byli na zawsze podłączeni do maszyny ze sprężonym powietrzem za pomocą rur.
Jarvik-7 został ostatecznie użyty jako środek stopgap dla pacjentów oczekujących na naturalne serca i dawał nadzieję, że nie będzie oczekiwania na przeszczepy. W 1998 roku Jarvik kontynuował prace nad samodzielnym urządzeniem, które ma być wszczepione do chorego serca, aby działało prawidłowo.
proces produkcyjny
-
1 Większość komponentów jest wykonywana zgodnie z niestandardowymi specyfikacjami przez producentów zewnętrznych, w tym sklepy maszynowe i producenci płytek drukowanych. Świńskie zastawki są wszyte wewnątrz przeszczepów szwami w firmie urządzeń medycznych, która specjalizuje się w zastawkach serca.
po uzyskaniu wszystkich komponentów system LVAD jest montowany i testowany, aby zapewnić, że każde urządzenie spełnia wszystkie specyfikacje. Po przetestowaniu LVAD może być sterylizowany i pakowany do wysyłki.
formowanie części poliuretanowych
- 2 niektórzy producenci sztucznego serca produkują własne części poliuretanowe. W jednym procesie stosuje się opatentowany płynny roztwór, który wlewa się na trzpień ceramiczny warstwa po warstwie. Każda warstwa jest podgrzewana i suszona, aż do uzyskania pożądanej grubości. Część jest następnie usuwana z trzpienia i sprawdzana. W przeciwnym razie producent zewnętrzny stosuje proces formowania wtryskowego lub formowania próżniowego w połączeniu ze spawaniem radiowym.
montaż
- 3 każde sztuczne serce zajmuje kilka dni, aby złożyć i przetestować. Proces montażu odbywa się w czystym pomieszczeniu, aby uniknąć zanieczyszczenia. Każde sztuczne serce składa się do 50 elementów, które są łączone za pomocą specjalnych klejów. Kleje te wymagają utwardzania w wysokich temperaturach. Kilka operacji montażowych odbywa się równolegle, w tym montaż obudowy silnika i komponentów, montaż rury przezskórnej i mocowanie płyt popychacza do membrany poliuretanowej. Podsystemy te są indywidualnie sprawdzane, a następnie następuje końcowy montaż kompletnego systemu. Przeszczepy są montowane oddzielnie i mocowane podczas pracy.
testowanie
- 4 po zakończeniu montażu każde urządzenie jest testowane za pomocą specjalnego sprzętu, który symuluje ciśnienie w ciele. Wszystkie elementy elektroniczne są testowane za pomocą elektronicznego sprzętu testowego, aby zapewnić prawidłowe działanie wszystkich obwodów.
Sterylizacja / pakowanie
- 5 Po przetestowaniu i przejściu sztucznego serca jest ono wysyłane do usługi zewnętrznej w celu sterylizacji. Każde urządzenie jest zamknięte w plastikowych tacach i zwrócone do producenta serca. Następnie jest pakowany w niestandardowe walizki, aby chronić go przed zanieczyszczeniem i zapobiegać uszkodzeniom.
Kontrola jakości
większość komponentów przeszła już kontrolę, zanim dotarły do producenta serca. Niektóre elementy są nadal kontrolowane wymiarowo, ponieważ wymagają wąskich tolerancji-rzędu milionowych części cala, co wymaga specjalnych narzędzi pomiarowych. Aby spełnić przepisy FDA, każdy komponent (w tym kleje) używany w procesie jest kontrolowany przez partię i numer seryjny, dzięki czemu możliwe są problemy ze śledzeniem.
produkty uboczne/odpady
złom tytanu jest odzyskiwany i poddawany recyklingowi po przetopieniu i przekształceniu. W przeciwnym razie powstaje niewiele odpadów, ponieważ większość komponentów przeszła kontrolę przed opuszczeniem różnych producentów. Inne wadliwe części są odrzucane. Po użyciu urządzenia przez pacjenta, jest on wysyłany z powrotem do producenta serca do analizy w celu poprawy projektu.
przyszłość
w ciągu następnej dekady na rynku pojawi się szereg nowych urządzeń. Naukowcy z Pennsylvania State University opracowują elektromechaniczne serce zasilane energią o częstotliwości radiowej, która jest przesyłana przez skórę. Silnik napędza płyty pchające, które naprzemiennie naciskają na plastikowe worki wypełnione krwią, aby symulować pompowanie. Pacjenci noszą ze sobą akumulator w ciągu dnia i śpią z urządzeniem podłączonym do gniazdka elektrycznego. To sztuczne serce będzie testowane na ludziach do 2001 roku.
kilka grup badawczych opracowuje pompy, które cyrkulują krew w sposób ciągły, a nie wykorzystują działania pompującego, ponieważ pompy te są mniejsze i bardziej wydajne. W Australii Micromedical Industries Limited opracowuje rotacyjną pompę krwi o przepływie ciągłym, która ma zostać wszczepiona człowiekowi do 2001 roku. Wydział kardiologii Ohio State University opracowuje plastikową pompę wielkości krążka hokejowego, która jest samoregulująca. Pompa ta jest wszczepiana pacjentom przez kilka tygodni, aż do odzyskania własnego serca.
Thermo Cardiosystems, Inc. pracuje również nad LVAD z pompą rotacyjną o ciągłym przepływie), która ma zostać wszczepiona gdzieś w 2000 roku, oraz LVAD z pompą odśrodkową o ciągłym przepływie. Ta ostatnia jest jeszcze we wczesnej fazie rozwoju, ale planuje się, że będzie to pierwsza na świecie pompa bez łożysk, co oznacza, że nie będzie miała żadnych części, które się zużywają. Osiąga się to poprzez magnetyczne zawieszenie wirnika pompy. Oba te urządzenia będą dostępne z przezskórnym transferem energii, co oznacza, że urządzenia będą w pełni wszczepialne.
z mniejszą liczbą serc dawców staje się dostępna, inni również rozwijają sztuczne serce, które jest stałym zamiennikiem. Te zamienniki mogą być w postaci urządzenia wspomagającego lewą komorę lub całkowitego sztucznego serca, w zależności od stanu fizycznego pacjenta. LVADs są opracowywane przez wynalazcę Roberta Jarvika i znanego kardiochirurga Michaela Debakeya. Total artificial hearts są wspólnie opracowywane przez Texas Heart Institute i Abiomed, Inc. w Massachusetts. W Japonii naukowcy opracowują sztuczne serca oparte na silikonowym systemie zaworów kulowych i pompie odśrodkowej z układem łożyskowym wykonanym z elementów ceramicznych z tlenku glinu i polietylenu.
opracowywane są również alternatywy dla sztucznych serc i pomp wspomagających pracę serca. Na przykład wynaleziono specjalny zacisk, który zmienia kształt chorego serca, co ma poprawić wydajność pompowania nawet o 30%. Takie urządzenie wymaga minimalnej inwazyjnej operacji wszczepienia.
gdzie dowiedzieć się więcej
„Urządzenie pomagające sercom. Cincinnati Enquirer (7 Listopada 1999).
Castor, Tasha. „Jednostka Kardiologiczna Ohio State University nastawiona na pompowanie serca.”The Lantern (6 Maja 1999).
” Electric Hearts by 2005.”Popular Mechanics (Marzec 1997).
Guglotta, Facet. „Upbeat na ludzkich sercach: ulepszone urządzenia zapisać te zbyt III do przeszczepu.”The Washington Post (June 28, 1999): AOl.
Guy, T. Sloane. „Ewolucja i obecny Status Total Artificial Heart: The Search Continues.”Asaio Journal (January-February 1998): 28-33.
Hall, Celia. „Pompa Wielkości Kciuka Może Zmniejszyć Śmierć Serca.”The Daily Telegraph (13 Września 1999): 11.
Hesman, Tina. „Pompa przynosi nowe oczekiwania wobec sztucznego serca.”Omaha World-Herald (12 Grudnia 1999).
Hopkins, Elaine. „Urządzenie pozwala pacjentowi serca czekać na przeszczep w domu.”Journal Star (30 Listopada 1999).
Kinney, David. „Skuteczne Sztuczne Serce Wydaje Się W Zasięgu Ręki.”The Los Angeles Times (23 Stycznia 2000).
Kolff, William. „Early Years of Artificial Organs at the Cleveland Clinic: Part II: Open Heart Surgery and Artificial Heart Surgery.”Asaio Journal (May-June 1998): 123-128.
Kolff, William. „Potrzeba łatwiejszego wytwarzania sztucznych serc i urządzeń wspomagających oraz jak ta potrzeba może być zaspokojona przez technikę formowania próżniowego.”Asaio Journal (January-February 1998): 12-27.
Kunzig, Robert. „The Beat Goes On.”Discover (January 2000): 33-34.
M2 Komunikacji. „Udane testy zgodności krwi dla sztucznego serca Micromedical.”M2 PressWIRE (26 Marca 1999).
Phillips, Winfred. „The Artificial Heart: History and Current Status.”Journal of Biomechanical Engineering (November 1993): 555-557.
Takami, Y. et al. „Obecny postęp w rozwoju całkowicie wszczepialnego żyroskopowego sztucznego serca.”Asaio Journal (May-June 1998): 207-211.
Wilson, Steve. „Wyścig życia i śmierci z czasem. „Arizona Republic (14 Listopada 1999).
Yambe, T. et al. „Opracowanie całkowitego sztucznego serca z ekonomicznymi i trwałymi zaletami.”The International Journal of Artificial Organs (1998): 279-284.
Inne
” postępy w rozwoju sztucznego serca.”http://www.uts.edu.au/new/archives/l999/February/02.html (29 grudnia 2000).
— Laurel M. Sheppard




