Corazón artificial
Antecedentes
Un corazón natural tiene dos bombas, cada una con dos cámaras. La aurícula derecha bombea sangre sin oxígeno del cuerpo hacia el ventrículo derecho, que la bombea a los pulmones. La aurícula izquierda envía sangre aireada de los pulmones al ventrículo izquierdo, que la bombea hacia el cuerpo. Con cada latido del corazón, las dos aurículas se contraen juntas, seguidas de los grandes ventrículos.
La insuficiencia cardíaca congestiva, que es la capacidad cada vez menor del corazón para bombear sangre, es una de las principales causas de muerte. Esta enfermedad es causada por daños repentinos de ataques cardíacos, deterioro de infecciones virales, mal funcionamiento de las válvulas, presión arterial alta y otros problemas. Según la Asociación Americana del Corazón, se estima que cinco millones de estadounidenses viven con insuficiencia cardíaca y se diagnostican más de 400,000 casos nuevos cada año. Alrededor del 50% de todos los pacientes mueren en un plazo de cinco años. Las enfermedades cardíacas le costaron a la industria de la salud de los Estados Unidos alrededor de 9 95 mil millones en 1998.
Aunque los medicamentos y las técnicas quirúrgicas pueden ayudar a controlar los síntomas, la única cura para la insuficiencia cardíaca es un trasplante de órgano. En 1998, alrededor de 7,700 estadounidenses estaban en la lista nacional de trasplantes de corazón, pero solo el 30% recibió trasplantes. Por lo tanto, se han desarrollado corazones artificiales y dispositivos de ayuda a la bomba como posibles alternativas.
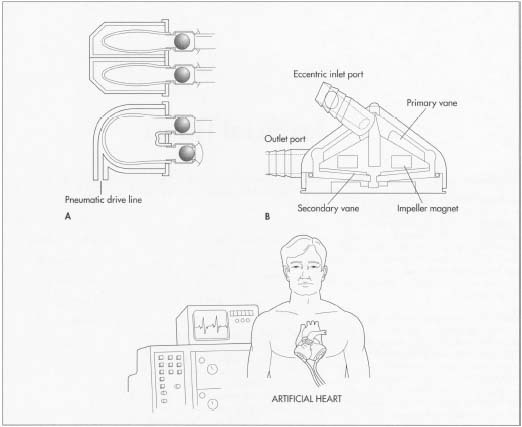
Un corazón artificial mantiene la circulación sanguínea y la oxigenación del corazón durante diversos períodos de tiempo. El corazón artificial ideal debe latir 100.000 veces cada 24 horas sin necesidad de lubricación ni mantenimiento y debe tener una fuente de energía constante. También debe bombear más rápido o más lento dependiendo de la actividad del paciente sin causar infección ni coágulos de sangre.
Los dos tipos principales de corazones artificiales son la máquina corazón-pulmón y el corazón mecánico. El primer tipo consiste en un oxigenador y una bomba y se utiliza principalmente para mantener el flujo sanguíneo mientras se opera el corazón. Esta máquina solo puede funcionar durante unas pocas horas, ya que la sangre se daña después de más tiempo.
Un corazón mecánico está diseñado para reducir la carga de trabajo total de un corazón que ya no puede funcionar a su capacidad normal. Estos corazones consisten en equipos que pulsan la sangre entre los latidos del corazón o utilizan un ventrículo auxiliar artificial (dispositivo de asistencia para el ventrículo izquierdo, LVAD) que bombea una parte del gasto cardíaco normal. Debido a que tales dispositivos generalmente resultan en complicaciones para el paciente, generalmente se han utilizado como reemplazo temporal hasta que se puedan obtener corazones naturales para el trasplante. En todo el mundo se han implantado unos 4.000 DAVI. El mercado de estos dispositivos se estima en $12 mil millones por año en los Estados unidos.
Historia
Desde finales del siglo XIX, los científicos han tratado de desarrollar un dispositivo mecánico que pudiera restaurar el oxígeno a la sangre y eliminar el exceso de dióxido de carbono, así como una bomba para suplantar temporalmente la acción del corazón. Pasaron casi 100 años antes de que John H. Gibbon Jr.usara en un ser humano la primera máquina de corazón y pulmón exitosa en 1953. Cuatro años más tarde, el primer corazón artificial (hecho de plástico) en el mundo occidental se implantó dentro de un perro. El Instituto Nacional del Corazón
estableció el programa de corazón artificial en 1964, lo que llevó al primer corazón artificial total para uso humano implantado en 1969.
El énfasis se desplazó a los sistemas de asistencia ventricular izquierda y a los materiales compatibles con sangre en 1970. Durante ese mismo año, se utilizó con éxito un DAVI. Sin embargo, el desarrollo de bombas de sangre continuó y los dispositivos se hicieron más pequeños, ligeros, aceptables y clínicamente exitosos. También se desarrollaron una serie de bombas de poliuretano y plástico de larga duración. Durante la década de 1980, la Administración de Alimentos y Medicamentos (FDA) impuso reglas más restrictivas a la Ley de Estándares de Dispositivos Médicos, lo que llevó a mayores costos de desarrollo. Muchos grupos de investigación tuvieron que abandonar, y solo quedan unos pocos.
Quizás el científico más famoso es el Dr. Robert Jarvik, quien inventó un corazón artificial llamado Jarvik-7. Este dispositivo, hecho de aluminio y plástico, reemplazó las dos cámaras inferiores del corazón natural y utilizó dos diafragmas de goma para la acción de bombeo. Un compresor externo del tamaño de un refrigerador mantuvo el corazón artificial latiendo. Barney Clark fue el primer paciente en recibir este corazón. Sobrevivió 112 días antes de que las complicaciones físicas causadas por el implante se quitaran la vida. En 1986, William Schroeder se convirtió en el segundo receptor de Jarvik-7, sobreviviendo durante unos 20 meses.
La comunidad médica se dio cuenta de que un corazón completamente implantable podría evitar los problemas de movilidad e infección causados por el Jarvik-7. En 1988, los Institutos Nacionales de Salud comenzaron a financiar el desarrollo de esos corazones y en 1991 apoyaron un programa de ese tipo por un total de 6 millones de dólares. Tres años más tarde, se puso a disposición un LVAD implantable eléctrico y alimentado por batería. En 1999, Charlie Chappis se convirtió en el primer paciente dado de alta de un hospital con un dispositivo de este tipo. Actualmente se están probando otros corazones artificiales de varios diseños.
Materias primas
Un corazón artificial o LVAD está hecho de metal, plástico, cerámica y partes de animales. Se utiliza una aleación de titanio, aluminio y vanadio para la bomba y otras piezas metálicas porque es biocompatible y tiene propiedades estructurales adecuadas. Las piezas de titanio se funden en un procesador de titanio especializado. A excepción de las superficies que entran en contacto con la sangre, el titanio se mecaniza con un acabado específico. Las superficies en contacto con la sangre reciben un revestimiento especial de microesferas de titanio que se unen permanentemente a la superficie. Con este recubrimiento, las células sanguíneas se adhieren a la superficie, creando un revestimiento vivo.
Un diafragma en contacto con la sangre dentro de la bomba está hecho de un tipo especial de poliuretano que también está texturizado para proporcionar adherencia a las células sanguíneas. Dos injertos tubulares están hechos de poliéster (que se utilizan para unir el dispositivo a la aorta) y las válvulas son válvulas cardíacas reales que se extraen de un cerdo. Otras partes que componen el motor están hechas de titanio u otros metales y cerámica.
Diseño
Hay varios problemas críticos al diseñar un LVAD. La dinámica de fluidos del flujo sanguíneo debe entenderse para que se bombee suficiente sangre y no se creen coágulos de sangre. Se deben elegir materiales que sean biocompatibles; de lo contrario, la bomba podría fallar. La eficiencia del motor debe optimizarse para que se genere un calor mínimo. Debido a un posible rechazo, el volumen total y la superficie de todo el dispositivo deben mantenerse lo más pequeños posible. Un LVAD típico pesa alrededor de 2,4 lb (1.200 g) y tiene un volumen de 1,4 pintas (660 ml).
Robert Jarvik nació el 11 de mayo de 1946, en Midland, Michigan, y se crió en Stamford, Connecticut. Ingresó en la Universidad de Siracusa de Nueva York en 1964, estudiando arquitectura y dibujo mecánico. Después de que su padre desarrollara una enfermedad cardíaca, Jarvik cambió a pre-medicina. Se graduó en 1968 con una licenciatura en zoología, pero fue rechazado por las escuelas de medicina de los Estados Unidos. Ingresó en la Universidad de Bolonia en Italia, pero se fue en 1971 a la Universidad de Nueva York, donde obtuvo una maestría en biomecánica ocupacional.
Jarvik solicitó un trabajo en la Universidad de Utah. El director del Instituto de Ingeniería Biomédica y División de Órganos Artificiales, Willem Kolff, había estado desarrollando un corazón artificial desde mediados de la década de 1950. Jarvik comenzó como su asistente de laboratorio, obteniendo su título de médico en 1976.
El 2 de diciembre de 1982, los médicos trasplantaron el primer corazón artificial a un ser humano. Este dispositivo de plástico y aluminio, el Jarvik-7, fue implantado en Barney Clark, quien sobrevivió 112 días después de la operación. Varios otros pacientes recibieron corazones Jarvik-7, pero ninguno vivió más de 620 días. Los principales beneficios eran que no habría una espera para un corazón humano y no había posibilidad de rechazo. La trampa obvia es que los pacientes estaban conectados para siempre a una máquina de aire comprimido a través de tubos.
El Jarvik-7 se utilizó finalmente como medida provisional para pacientes que esperaban corazones naturales y proporcionó esperanza de que no habría una espera para trasplantes. En 1998, Jarvik continuó trabajando en un dispositivo autónomo que se implantaría en el corazón enfermo de una persona para que funcionara correctamente.
El Proceso de Fabricación
-
1 La mayoría de los componentes están hechos según especificaciones personalizadas por fabricantes externos, incluidos talleres de máquinas y fabricantes de placas de circuitos impresos. Las válvulas porcinas se cosen dentro de los injertos con suturas en una empresa de dispositivos médicos que se especializa en válvulas cardíacas.
Una vez que se obtienen todos los componentes, el sistema LVAD se ensambla y prueba, para garantizar que cada dispositivo cumpla con todas las especificaciones. Una vez probado, el LVAD se puede esterilizar y empaquetar para su envío.
Formando las piezas de poliuretano
- 2 Algunos fabricantes de corazón artificial fabrican sus propias piezas de poliuretano. Un proceso utiliza una solución líquida patentada que se vierte sobre un mandril de cerámica capa por capa. Cada capa se calienta y se seca hasta alcanzar el grosor deseado. La pieza se retira del mandril y se inspecciona. De lo contrario, un fabricante externo utiliza un proceso de moldeo por inyección o moldeo al vacío combinado con soldadura por radiofrecuencia.
Montaje
- 3 Cada corazón artificial tarda varios días en armarse y probarse. El proceso de montaje se realiza en una sala limpia para evitar la contaminación. Cada corazón artificial consta de hasta 50 componentes que se ensamblan utilizando adhesivos especiales. Estos adhesivos requieren curado a altas temperaturas. Varias operaciones de montaje se realizan en paralelo, incluido el montaje de la carcasa y los componentes del motor, el montaje del tubo percutáneo y la fijación de las placas empujadoras al diafragma de poliuretano. Estos subsistemas se inspeccionan individualmente, luego se produce el ensamblaje final del sistema completo. Los injertos se ensamblan por separado y se fijan durante la operación.
Pruebas
- 4 Una vez completado el ensamblaje, cada dispositivo se prueba con un equipo especial que simula las presiones en el cuerpo. Todos los componentes electrónicos se prueban con equipos de prueba electrónicos para garantizar el funcionamiento adecuado de todos los circuitos.
Esterilización / embalaje
- 5 Después de que el corazón artificial se prueba y pasa, se envía a un servicio externo para la esterilización. Cada dispositivo se sella en bandejas de plástico y se devuelve al fabricante del corazón. Luego se empaqueta en maletas personalizadas para protegerlo de la contaminación y evitar daños.
Control de calidad
La mayoría de los componentes ya han pasado la inspección antes de llegar al fabricante del corazón. Algunos componentes aún se inspeccionan dimensionalmente, ya que requieren tolerancias ajustadas, del orden de las millonésimas de pulgada, lo que requiere herramientas de medición especiales. Para cumplir con las regulaciones de la FDA, cada componente (incluidos los adhesivos) utilizado en el proceso está controlado por lote y número de serie para que sea posible que surjan problemas de seguimiento.
Subproductos / Residuos
La chatarra de titanio se recupera y recicla después de su refundición y refundición. De lo contrario, se producen pocos residuos, ya que la mayoría de los componentes han pasado la inspección antes de abandonar los diversos fabricantes. Se desechan otras piezas defectuosas. Una vez que un paciente ha utilizado un dispositivo, se envía de vuelta al fabricante del corazón para que lo analice y mejore el diseño.
El futuro
En la próxima década, una serie de nuevos dispositivos saldrán al mercado. Investigadores de la Universidad Estatal de Pensilvania están desarrollando un corazón electromecánico alimentado por energía de radiofrecuencia que se transmite a través de la piel. Un motor acciona placas de empuje, que se alternan al presionar contra sacos de plástico llenos de sangre para simular el bombeo. Los pacientes llevan un paquete de baterías durante el día y duermen con el dispositivo conectado a una toma de corriente eléctrica. Este corazón artificial será probado en humanos para el año 2001.
Varios grupos de investigación están desarrollando bombas que hacen circular la sangre de forma continua, en lugar de utilizar una acción de bombeo, ya que estas bombas son más pequeñas y más eficientes. En Australia, Micromedical Industries Limited está desarrollando una bomba de sangre rotativa de flujo continuo, que se espera implantar en un ser humano en 2001. El departamento de cardiología de la Universidad Estatal de Ohio está desarrollando una bomba de plástico del tamaño de un disco de hockey que se autorregula. Esta bomba se implanta en los pacientes durante varias semanas hasta que su propio corazón se recupera.
Thermo Cardiosystems, Inc. también está trabajando en un LVAD con una bomba rotativa de flujo continuo), que se espera que se implemente en algún momento del año 2000, y un LVAD con una bomba centrífuga de flujo continuo. Esta última aún se encuentra en una fase temprana de desarrollo, pero se planea que sea la primera bomba sin soporte del mundo, lo que significa que no tendrá piezas que se desgasten. Esto se logra suspendiendo magnéticamente el rotor de la bomba. Ambos dispositivos estarán disponibles con transferencia de energía transcutánea, lo que significa que los dispositivos serán completamente implantables.
Con menos corazones de donantes disponibles, otros también están desarrollando un corazón artificial que es un reemplazo permanente. Estos reemplazos pueden ser en forma de un dispositivo de asistencia para el ventrículo izquierdo o un corazón artificial total, dependiendo de la condición física del paciente. Los LVAD están siendo desarrollados por el inventor Robert Jarvik y el reconocido cirujano cardíaco Michael DeBakey. Corazones artificiales totales están siendo desarrollados conjuntamente por el Instituto del Corazón de Texas y Abiomed, Inc. en Massachusetts. En Japón, los investigadores están desarrollando corazones artificiales totales basados en un sistema de válvula de bola de silicona y una bomba centrífuga con un sistema de cojinetes hecho de componentes de cerámica de alúmina y polietileno.
También se están desarrollando alternativas a los corazones artificiales y las bombas de asistencia cardíaca. Por ejemplo, se ha inventado una pinza especial que cambia la forma de un corazón enfermo, lo que se espera que mejore la eficiencia de bombeo hasta en un 30%. Un dispositivo de este tipo requiere una cirugía invasiva mínima para implantarse.
Dónde obtener más información
Publicaciones periódicas
Bonfield, Tim. «Dispositivo para Ayudar a los Corazones.»Cincinnati Enquirer (7 de noviembre de 1999).
Castor, Tasha. «La Unidad de Cardiología de la Universidad Estatal de Ohio Probará la Bomba Cardíaca.»The Lantern (6 de mayo de 1999).
» Corazones eléctricos para 2005.»Popular Mechanics (marzo de 1997).
Gugliotta, Guy. «Upbeat on Man-Made Hearts: Improved Devices Save Those Too III for Transplant.»The Washington Post (28 de junio de 1999): AOl.
Guy, T. Sloane. «Evolución y Estado Actual del Corazón Artificial Total: La Búsqueda Continúa.»ASAIO Journal (Enero-febrero de 1998): 28-33.
Hall, Celia. «La Bomba Del Tamaño De Un Pulgar Puede Reducir Las Muertes Cardíacas.»The Daily Telegraph (13 de septiembre de 1999): 11.
Hesman, Tina. «La Bomba Trae Nuevas Expectativas para el Corazón Artificial.»Omaha World-Herald (12 de diciembre de 1999).
Hopkins, Elaine. «El Dispositivo Permite al Paciente Cardíaco Esperar el Trasplante en Casa.»Journal Star (30 de noviembre de 1999).
Kinney, David. «El Corazón Artificial Efectivo Parece Estar Al Alcance De La Mano.»The Los Angeles Times (23 de enero de 2000).
Kolff, William. «Early Years of Artificial Organs at the Cleveland Clinic: Part II: Open Heart Surgery and Artificial Hearts.»ASAIO Journal (Mayo-junio de 1998): 123-128.
Kolff, William. «La Necesidad de una Fabricación Más Fácil de Corazones Artificiales y Dispositivos de Asistencia y Cómo Se Puede Satisfacer Esta Necesidad con la Técnica de Moldeo al Vacío.»ASAIO Journal (Enero-febrero de 1998): 12-27.
Kunzig, Robert. «El Ritmo Continúa.»Discover (Enero de 2000): 33-34.
Comunicaciones M2. «Pruebas de Compatibilidad Sanguínea Exitosas para el Corazón Artificial de Micromedical.»M2 PressWIRE (26 de marzo de 1999).
Phillips, Winfred. «The Artificial Heart: History and Current Status.»Journal of Biomechanical Engineering (noviembre de 1993): 555-557.
Takami, Y. et al. «Progreso Actual en el Desarrollo de un Corazón Artificial Giroscópico Totalmente Implantable.»ASAIO Journal (Mayo-junio de 1998): 207-211.
Wilson, Steve. «Una Carrera de Vida y Muerte Contra El Tiempo. «Arizona Republic (14 de noviembre de 1999).
Yambe, T. et al. «Desarrollo de Corazón Artificial Total con Ventajas Económicas y de Durabilidad.»The International Journal of Artificial Organs (1998): 279-284.
Otros
» Progreso en el Desarrollo de un Corazón Artificial.»http://www.uts.edu.au/new/archives/l999/February/02.html (29 de diciembre de 2000).
— Laurel M. Sheppard




